010-84279654
-
扫一扫关注微信公众号:

010-84279654
扫一扫关注微信公众号:

什么是缓冲溶液?缓冲液(Buffer solution)通常是由「弱酸及其共轭碱」或「弱碱及其共轭酸」缓冲对所组成的溶液,能够在加入一定量其他物质时减缓pH的改变。以生物实验中最常用的一种缓冲液PBS为例,是由Na2HPO4、KH2PO4组成的缓冲对,在PH5.8-8.0范围内有较强的缓冲能力。
缓冲原理
假设缓冲溶液里含有弱酸HA以及它的共轭碱 。在溶液里发生的质子反应为:
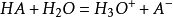
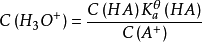
水合氢离子的浓度取决于弱酸与其共轭碱的浓度比。当加入少量强碱时,酸被中和,导致了氢氧根离子在溶液中很少累积,从而 的浓度增加, 的浓度减少。可以看到,虽然加入了强碱,但是溶液里的氢氧根离子变化很少,同时,
浓度较大,相对的变化小,两者比值几乎无变化,因此根据公式,水合氢离子的浓度变化很小。加入弱酸则是同样的道理。由于在大浓度基数上的微小变化不会改变比值,也因此维持了体系内氢离子和氢氧根离子浓度的平衡。
缓冲溶液的选择与计算
为了保证缓冲溶液有足够强的缓冲能力,在配制缓冲溶液时,需要做到:
为使共轭酸碱对的浓度比接近于1,应根据所需要维持的pH范围选择合适的缓冲对,使其中的弱酸的PKa等于或接近于所要求的pH。
例如,生物培养液中需用PH=7.0的缓冲溶液,已知H2PO4-的pKa2=7.21,因此,H2PO4—HPO42-是可以选择的合适的缓冲对。如若配制PH=9.0的缓冲溶液,则可选择NH3·H2O-NH4Cl缓冲对(pKa(NH4+)=9.25)。可见弱酸的Ka是选择缓冲溶液的主要依据,表中列出了几种常用的缓冲溶液。
更多精彩内容请搜索、关注公众号:“活水源认证咨询培训服务平台”或“huoshuiyuan001”
